Гиалуроновая кислота в коррекции возрастных изменений кожи: оптимальные физико-химические характеристики, модификации и персонализированные стратегии
H.П. Михайлова1, Д.И. Знатдинов1, М.A. Петрий2, И.B. Борзова3
1 AHO «Международный научно-исследовательский центр инновационных технологий Мартинекс», Москва, Россия
2 ФГБУ ДПO «Центральная государственная медицинкская академия» Управления делами Президента Российской Федерации, Москва, Россия
3 AHHO BO Hаучно-исследовательский центр «Санкт-Петербургский Институт биорегуляции и геронтолоrии», Санкт-Петербурr, Россия
РЕЗЮМЕ
Гиалуроновая кислота (ГК) – ключевой биополимер в инъекционной косметологии, регулирующий процессы регенерации, воспаления и гидратации тканей. Её функциональная полиморфность, обусловленная вариабельностью молекулярной массы (ММ), пространственной организации и взаимодействий с рецепторами, определяет двойственность биологических эффектов. Такая дихотомия делает ГК центральным объектом исследований в биомедицине и косметологии, где управление её свойствами открывает пути к персонализированным терапевтическим стратегиям. Современная инъекционная косметология сталкивается с вызовами, связанными с ограничениями в использовании нативной гиалуроновой кислоты и традиционных филлеров на основе сшитой ГК. Быстрая биодеградация нативной ГК под действием активных форм кислорода, азота, а также гиалуронидаз дополнительно снижает долгосрочный эффект. Несмотря на способность корректировать объёмные дефекты, филлеры для контурной пластики не воздействуют на патогенетические механизмы старения, а их применение сопряжено с риском побочных реакций из‑за остаточного содержания кросс‑линкеров. Эти проблемы актуализируют поиск инновационных подходов к стабилизации полимера, контролю его ММ и интеграции биоактивных компонентов для синергии объемной коррекции и биохимического воздействия. Перспективу представляют методы твердофазной модификации ГК – механохимическое сшивание с биорегуляторами, исключающее токсичные реагенты и обеспечивающее контролируемую доставку активов. Актуальность работы обусловлена необходимостью перехода от симптоматической коррекции к патогенетически обоснованным вмешательствам в инъекционной косметологии. Несмотря на обширный спектр существующих препаратов, выбор оптимальных форм ГК часто основывается на эмпирических данных, что приводит к вариативности результатов и риску осложнений. Систематизация современных научных данных о влиянии молекулярной массы, постсинтетических модификаций и рецепторного взаимодействия ГК на эффективность процедур является ключевым шагом для перехода к патогенетически обоснованным протоколам, минимизирующим риск нежелательных явлений.
КЛЮЧЕВЫЕ СЛОВА: гиалуроновая кислота, инъекционная косметология, молекулярная масса, твердофазная модификация, anti‑age терапия.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы заявляют об отсутствии конфликта интересов.
Hyaluronic acid in the improvement of skin aging: optimal physicochemical characteristics, modifications, and personalized strategies
N.P. Mikhailova1, D.I. Znatdinov1, M.A. Petriy2, I.V. Borzova3
1 Martinex International Research Center for Innovative Technologies, Moscow, Russia
2 Central State Medical Academy of the Administrative Department of the President of the Russian Federation, Moscow, Russia
3 Saint Petersburg Institute of Bioregulation and Gerontology, Saint Petersburg, Russia
SUMMARY
Hyaluronic acid (HA) is a key biopolymer in injection cosmetology, regulating processes of tissue regeneration, inflammation, and hydration. Its functional polymorphism, determined by variability in molecular weight (MW), spatial organization, and receptor interactions, defines the duality of its biological effects. This dichotomy positions HA as a central focus of research in biomedicine and cosmetology, where controlling its properties opens pathways to personalized therapeutic strategies. Modern injection cosmetology faces challenges related to limitations in the use of native hyaluronic acid and traditional cross‑linked HA fillers. Rapid biodegradation of native HA by reactive oxygen and nitrogen species, as well as hyaluronidases, further diminishes long‑term efficacy. Despite their ability to correct volume deficits, dermal fillers do not address the pathogenetic mechanisms of aging, and their application carries risks of adverse reactions due to residual cross‑linker content. These problems highlight the need for innovative approaches to polymer stabilization, MW control, and the integration of bioactive components to synergize volumetric correction with biochemical impact. Solid‑phase modification methods for HA hold promise – specifically, mechanochemical cross‑linking with bio‑regulators, which eliminates toxic reagents and ensures controlled delivery of active agents. The relevance of this work stems from the necessity to transition from symptomatic correction to pathogenetically‑grounded interventions in injection cosmetology. Despite the broad spectrum of existing preparations, the selection of optimal HA forms is often based on empirical data, leading to variable outcomes and complication risks. Systematizing current scientific evidence on the influence of HA molecular weight, post‑synthetic modifications, and receptor interactions on procedural efficacy is a crucial step towards establishing pathogenetically‑grounded protocols that minimize the risk of complications.
KEYWORDS: hyaluronic acid, injection cosmetology, molecular weight, solid‑phase modification, anti‑age therapy.
CONFLICT OF INTEREST. The authors declare no conflict of interest.
Введение
Гиалуроновая кислота (ГК) – уникальный гликозаминогликан, составляющий основу внеклеточного матрикса кожи и обеспечивающий её структурную целостность, гидратацию и механическую устойчивость. Её молекула, состоящая из повторяющихся дисахаридных единиц (D‑глюкуроновой кислоты и N‑ацетилглюкозамина), обладает исключительной гидрофильностью, что формирует гелеобразный матрикс, ответственный за тургор и эластичность тканей. В организме человека весом 70 кг содержится около 15 г ГК, треть которой ежедневно обновляется, подчёркивая её критическую роль в поддержании гомеостаза кожи [1]. С возрастом синтез эн- догенной ГК снижается: к 50 годам её концентрация в дерме падает на 30–50 %, что коррелирует с потерей объёма, а также структурной деградацией покровных тканей. Эти изменения ассоциированы с различными факторами, связанными с процессом старения, что делает ГК одной из ключевых мишеней для anti‑age терапии в инъекционной косметологии [2] [3] [4].
Гиалуроновая кислота (ГК) выступает ключевым регулятором в разнообразных биологических процессах. Её способность взаимодействовать с клеточными рецепторами и внеклеточными молекулами‑партнёрами определяет развитие органов и тканей, модулирует ответ на повреждение и воспаление, влияет на клеточную миграцию, онкогенез и резистентность опухолей. Примечательно, что в научных работах часто отмечается парадоксальная двойственность биологических эффектов ГК: например, она может проявлять как провоспалительные, так и противовоспалительные свойства, стимулировать или подавлять пролиферацию и миграцию клеток [5]. В водных растворах ГК формирует двойную спиральную конфигурацию, стабилизированную межмолекулярными водородными связями между ацетамидной группой и карбоксильной группой, а также за счет гидрофобных взаимодействий между отдельными участками молекулы. В условиях высокой концентрации молекулы ГК образуют сетчатую структуру, демонстрирующую эластичность благодаря процессам самоассоциации и пространственным эффектам. При направленном механическом воздействии фрагменты сети переориентируются, что приводит к проявлению вязкостных свойств, при этом часть межмолекулярных связей сохраняется. Комбинация этих характеристик обеспечивает формирование трехмерной вязкоупругой матрицы, играющей ключевую роль в биомеханике тканей [6]. Структура ГК‑ матрикса дополнительно стабилизируется электростатическими и гидрофобными взаимодействиями со связывающимися молекулами. Такая организация ограничивает проникновение белков и макромолекул в матрикс либо существенно снижает скорость их диффузии за счет эффекта молекулярного просеивания. В физиологических условиях (pH ≈7.4) ГК существует в виде полианиона благодаря ионизации карбоксильных групп. Это свойство влияет на пространственное распределение катионных соединений (питательных веществ, электролитов и т. п.) посредством слабых электростатических взаимодействий [7]. Рецептор CD 44 демонстрирует селективность к ГК‑фрагментам пределенной длины, активируя сигнальные каскады при связывании с олигомерами строго заданного размера. Например, он подавляет LPS‑индуцированную активацию TLR в макрофагах, а связывание ГК с CD 44 ингибирует TLR 4‑зависимый ответ при сепсисе. CD 44 выступает корецептором для рецепторов тирозинкиназ, GPCR и LRP6, что указывает на сложное взаимодействие между ГК, TLR 4 и CD 44 [8]. В отличие от него, Toll‑подобные рецепторы TLR 2 и TLR 4 проявляют аффинность преимущественно к низкомолекулярным фрагментам ГК, образующимся, например, при тканевом повреждении или воспалении [9]. Эти рецепторы активируют сигнальные каскады, такие как NF‑κB и MAPK‑пути, запуская продукцию провоспалительных цитокинов (например, IL‑6, TNF‑α) и хемокинов [10]. Разнообразие пространственных конформаций ГК, зависящее от длины полимерной цепи, объясняет механизм избирательного распознавания молекул рецепторами [11]. Современные исследования позволили идентифицировать четыре фундаментальных механизма, лежащих в основе этой функциональной полиморфности [12]:
- Физико‑химические характеристики, включая молекулярную массу, концентрацию и пространственное распределение биополимеров;
- Постсинтетические модификации – ковалентные изменения, образование межмолекулярных сшивок и формирование надмолекулярных комплексов;
- Динамика метаболизма – баланс между синтезом и деградацией ГК, регулируемый параметрами микроокружения;
- Рецептор‑опосредованные сигнальные каскады, определяющие клеточный ответ.
Эти механизмы тесно взаимосвязаны. Так, метаболические превращения ГК непосредственно влияют на её размеры и физические свойства, а изменения микроокружения могут модулировать структуру сшивок и доступность рецепторных сайтов. Следовательно, биологическая роль ГК представляет собой динамическую систему, где локальные эффекты интегрируются в многоуровневую регуляцию – от клеточных процессов до функций целого организма.
Актуальность работы обусловлена растущим спросом на научно‑ориентированные подходы в косметологии. В отличие от метаболических и рецепторных механизмов, которые зависят от индивидуальных физиологических особенностей пациента, первые два параметра являются управляемыми переменными на этапе разработки и выбора гидрогеля на основе гиалуроновой кислоты. Таким образом, понимание взаимосвязи «структура–функция» в контексте физико‑химических свойств и модификаций ГК служит основой для доказательного подхода в инъекционной косметологии, обеспечивая баланс между эффективностью и безопасностью процедур. А понимание корреляции между ключевыми параметрами ГК и клиническим исходом позволяет избежать ятрогенных осложнений и оптимизировать схемы терапии для разных морфотипов старения.
Физико‑химические характеристики
Гиалуроновая кислота – высокогидратированная полиа- нионная макромолекула, для которой характерен широкий диапазон молекулярных масс: от 100 000 Да в сыворотке крови до 8000 000 Да в стекловидном теле [13]. Функциональные свойства ГК напрямую коррелируют с её молекулярной мас- сой (ММ), определяющей биодоступность, продолжительность действия и механизмы взаимодействия с тканевыми рецепторами [14]. Например, рецептор ГК (CD 44) участвует во многих физиологических и патологических процессах, взаимодействуя с ГК и активируя ключевые сигнальные каскады [15]. Молекулярная масса ГК определяет функциональную авидность его взаимодействия с рецепторами. Высокомолекулярная ГК, благодаря структурным особеностям, обеспечивает высокоавидное связывание, напротив, низакомолекулярная ГК, обладая меньшей авидностью, активирует часто противоположные сигналы [17].
Анализ образцов методом хроматографии установил молекулярный вес 2000–6000 кДа в кожных структурах. Значение 6000 кДа отражает не отдельные молекулы ГК, а их агрегаты или комплексы с другими компонентами матрикса. HAS 2 напрямую не производит такие длинные цепи, но in vivo условия способствуют объединению молекул, что и фиксируется методами в виде повышенной массы. Кроме того, эпидермальная ГК в ряде случаев имела несколько большую массу по сравнению с дермальной [16]. Однако, стоит учитывать и прогрессивное снижение размера биополимера в коже в результате процесса старения [18].
Полученные данные о ММ ГК в коже критически важны для разработки препаратов для инъекционной косметологии, так как от ММ зависят их биодоступность, механизм действия и конечный эффект. Высокомолекулярная ГК обладает противовоспалительными, антипролиферативными, антиангиоген- ными и иммуносупрессивными свойствами. Она ингибирует дифференцировку клеток, стимулирует их пролиферацию, участвует в регенерации тканей, заживлении ран, поддер- жании целостности эпителия, организации внеклеточного матрикса (ВКМ) и регуляции водного гомеостаза. В отличие от высокомолекулярной ГК, низкомолекулярная ГК проявляет иммуностимулирующие и ангиогенные свойства, индуцируя провоспалительные цитокины, хемокины, факторы роста. А олигосахариды ГК (4–16 кДа) могут стимулировать воспаление (в зависимости от типа клеток и патологии) [19–22].
В промышленности гиалуроновую кислоту (ГК) получают из двух основных источников: петушиных гребней и бактериальных культур, выращенных методом ферментации. Поскольку структура ГК, продуцируемой данными микроорганизмами, идентична ГК млекопитающих, штаммы Streptococcus equi, S. zooepidemicus используются для биосинтеза полимеров с ММ до 2 МДа. Генетическая модификация этих штаммов позволила увеличить ММ ГК до 3,5 МДа. Следует учитывать, что указанные числовые значения молекулярной массы могут варьироваться в различных литературных источниках в зависимости от используемого метода анализа. ГК также синтезируется рекомбинантными штаммами Bacillus subtilis, Escherichia coli, Lactococcus lactis и Agrobacterium sp. Эти системы экспрессируют стрептококковый ген гиалуронансинтазы и продуцируют ГК с ММ до 1 МДа но, несмотря на устранение рисков, связанных с использованием патогенов (например, снижение содержания остаточных эндотоксинов), такой молекулярный вес недостаточен для применения во многих терапевтических областях [23]. Исходя из вышесказанного, молекулярная масса гиалуроновой кислоты (ГК) в тканях среднестатистического человека может достигать показателя практически в 2 раза выше, чем полученная путем бактериального синтеза, даже с использованием генетически модифицированных штаммов. К тому же, подавляющее большинство образцов гиалуроновой кислоты – как экстрагированных из биологических источников, так и синтезированных микробиологически – представляют собой гетерогенные системы, содержащие макромолекулы с вариативной длиной цепи. Даже при относительной гомогенности по ММ речь всегда идет об усредненных значениях, величина которых варьируется в зависимости от выбранного метода анализа. Это методологическое разнообразие объясняет расхождения в ха- рактеристиках одного и того же продукта при использовании разных подходов к определению ММ. В медицинской практике ключевое значение приобретает применение фракционированных форм ГК с контролируемой молекулярной массой, где узкий диапазон ММ напрямую коррелирует с функциональной специализацией препарата. При этом стоимость сырья определяется не только источником происхождения, но и степенью полидисперсности материала. Технологии очистки, направленные на сужение молекулярно‑массового распределения, существенно увеличивают производственные затраты. Снижение полидисперсности требует многоступенчатых процессов, что объясняет высокую себестоимость фармакопейных препаратов по сравнению с техническими аналогами широкого фракционного состава [24].
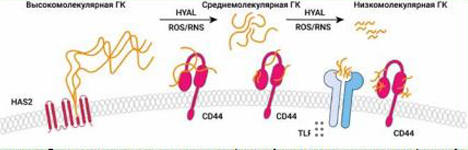
Учитывая физиологическую молекулярную массу ГК в структурах кожи, а также снижение ММ ГК, наблюдающееся в ходе производственного процесса инъекционных препаратов на основе ГК, использование исходного полимера с ММ ниже 2000–3500 кДа с концентрацией менее 1 % [25] с целью коррекции инволютивных изменений покровных тканей становится нерациональным ввиду того, что под действием ферментов (гиалуронидаз) и активных форм кислорода/азота, высокомолекулярная ГК и так подвергается биодеградации до низкомолекулярных фракций и олигомеров (рис. 1). Таким образом, целенаправленное использование высокомолекулярной ГК обеспечивает сохранение ее функционально значимых свойств, что критически важно для разработки эффективных биоматериалов для инъекционной косметологии.
|
|
|
Рисунок 1. Деградация высокомолекулярных фракций до низкомолекулярных фракций и олигомеров осуществляется под действием гиалуронидаз (HYAL), реактивных кислородных (ROS) и азотных (RNS) соединений. Биологическая роль образующихся дисахаридов in vivo требует дальнейшего изучения, так как экспериментальные данные об их функциональной активности остаются противоречивыми |
Однако нестабилизированная (нативная) ГК, несмотря на высокий молекулярный вес, демонстрирует ограниченный период полураспада, что препятствует реализации её полного биологического потенциала. Данный феномен обусловлен ускоренной биодеградацией молекулы под действием ферментативных систем, а также процессов неферментативного гидролиза. Быстрая деструкция полимерной цепи приводит к сокращению времени пребывания ГК в тканевом микроокружении, что лимитирует её способность к пролонгированному вза- имодействию с CD 44‑рецепторами и компонентами внеклеточного матрикса. Как следствие, наблюдается значительное снижение терапевтиче- ской эффективности, связанное с недостаточной продолжительностью модуляции ключевых тканевых процессов. Полученные данные подчеркивают необходимость применения методов стабилизации ГК для минимизации ферментативной чувствительности и увели- чения её резистентности к биотрансформации [26].
Постсинтетические модификации
Модификации ГК направлены на изменение биологической активности и других свойств материала. Основные химические преобразования затрагивают три функциональные группы: карбоксильную группу глюкуроновой кислоты, первичные и вторичные гидроксильные группы, а также N‑ацетильный фрагмент (после деамидирования) [27].
Различают два типа поперечных связей в биополимерах:
- Физические (электростатические взаимодействия, водородные связи) – разрушаются при нагреве с уменьшением модуля сдвига.
- Химические (ковалентные связи) – обеспечивают термостабильность, но при экстремальных температурах происходит необратимая деструкция.
Плотность сшивки определяется средней молекулярной массой участка цепи между узлами сетки. Этот параметр напрямую влияет на ключевые свойства: степень набухания, механическую прочность, эластичность, проницаемость и диффузионные характеристики.
Таким образом, комбинация химических и физических механизмов сшивки позволяет создавать гидрогели с програм- мируемыми свойствами для инъекционной косметологии [28]. Однако, филлеры на основе сшитой гиалуроновой кисло- ты (ГК), стабилизированной кросс‑линкинг агентами (BDDE, DVS, PEG), не являются истинными anti‑age инструментами, так как обеспечивают лишь симптоматическую коррекцию. Их механизм сводится к механическому заполнению дефектов, маскируя потерю объема тканей, без целевого воздействия на патогенез биологического старения [29, 30]. Кроме того, побочные реакции на остаточное содержание кросс‑линкеров, риск фиброзирования, гиперкоррекции и т.п. ограничивают их долгосрочное применение [31–33].
К тому же, реализация идеальной модели модификации ГК на практике встречается крайне редко или вовсе недостижима. Присутствие жидкой среды ограничивает контроль над процессом, приводит к побочным реакциям (гидролиз, окисление) и требует сложной очистки [34]. Метод твердофазного сшивания ГК биологически активными компонентами, решает эту проблему, исключая химические сшивающие реагенты, токсические растворители и катализаторы на всех этапах. Этот подход минимизирует участие воды и обеспечивает контакт компонентов на молекулярном или кластерном уровне, что может снизить побочные реакции. Механохимические реакции (этерификация, амидирование, модификация полисахаридов) открывают перспективы для синтеза биомедицинских материалов, недостижимые традиционными методами [35]. Твердофазный метод демонстрирует, что устранение воды из процесса сшивания позволяет избежать ключевых ограничений жидкофазной химии: гидролиза, неконтролируемой агрегации и остаточной токсичности. Это открывает путь для синтеза биосовместимых материалов с программируемыми свойствами, недостижимыми в водных средах.
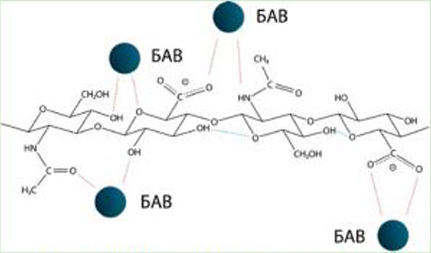
Модификация макромолекул в твердой фазе под давлением и сдвигом приводит к равномерному распределению связей по всей длине цепи. В отличие от жидкофазного процесса, где преобладают межмолекулярные связи (из‑за клубковой конформации), твердофазный метод обеспечивает более однородную структуру. Химическая модификация ГК путем присоединения боковых групп или конъюгации расширяет возможности ее сшивания с различными молекулами. Данный подход также актуален для создания пролекарств за счет ковалентного связывания активных молекул с ГК (рис. 2) [36, 37].
Низкомолекулярные биорегуляторы (1–5 мг/мл), включая аскорбилфосфат магния, рибофлавин, фолиевую кислоту, ретинол, α‑токоферол, медь, цинк, глутатион и аминокислоты (глицин, пролин, метионин, цистеин, лизин), нашли применение в твердофазной модификации высокомолекулярной ГК в рамках инъекционной косметологии [38].
Данный подход не только усиливает резистентность ГК к ферментативной биодеградации за счет стерической защиты гиалуронидаз‑чувствительных участков, но и модулирует фармакокинетический профиль системы, увеличивая период нахождения активных компонентов в тканях. Синергетический эффект комбинации проявляется в оптимизации биодоступности за счет контролируемого высвобождения агентов, опосредованного постепенным гидролизом полимерной матрицы, что способствует пролонгации терапевтического воздействия и минимизации частоты интервенций [39]. Персонализация таких систем, включая подбор компонентов с учетом специфики патологических процессов и индивидуальных биохимических маркеров, открывает пер- спективы для создания адресных терапевтических платформ в инъекционной косметологии с улучшенными клинико‑фар- макологическими характеристиками [40].
Таким образом, в контексте инъекционной косметологии критическое значение приобретает управление ММ и модификациями ГК. Традиционные филлеры на основе сшитой ГК, несмотря на способность корректировать объёмы, имеют ограничения в рамках anti‑age терапии. Инновационные подходы, такие как твердофазное сшивание, лишены этих недостатков. Они обеспечивают стерическую защиту от ферментативной деградации, контролируемое высвобождение биорегуляторов и синтез материалов с программируемыми свойствами без токсичных реагентов. Пример коммерческого препарата демонстрирует синергию объемной коррекции и биохимического воздействия на внеклеточный матрикс, что открывает путь к персонализированной терапии.
|
|
|
Рисунок 2. Твердофазная модификация ГК биологически активными веществами (БAB) |
Прогресс в понимании взаимосвязи «структура–функция» ГК позволяет разрабатывать доказательные косметологи- ческие стратегии. Оптимизация ММ, снижение полидис- персности и внедрение «умных» гидрогелей с адресной доставкой активов не только повышают эффективность процедур, но и минимизируют риски нежелательных реакций. Дальнейшие исследования должны быть направлены на изучение долгосрочных эффектов твердофазно модифицированной ГК, а также интеграцию индивидуальных биохимических параметров пациентов в дизайн терапевтических систем.
Список литературы / Reference
- Marinho A, Nunes C, Reis S. Hyaluronic Acid: A Key Ingredient in the Therapy of Inflammation. Biomol- ecules. 2021 Oct 15; 11 (10): 1518. DOI: 10.3390/biom11101518. PMID: 34680150; PMCID: PMC 8533685
- Fisher GJ, Varani J, Voorhees JJ. Looking older: fibroblast collapse and therapeutic implications. Arch Dermatol. 2008 May; 144 (5): 666–72. DOI: 10.1001/archderm.144.5.666. PMID: 18490597; PMCID: PMC 2887041
- López‑Otín C, Blasco MA, Partridge L, Serrano M, Kroemer G. Hallmarks of aging: An expanding universe. Cell. 2023 Jan 19; 186 (2): 243–278. DOI: 10.1016/j.cell.2022.11.001. Epub 2023 Jan 3. PMID: 36599349
- Garantziotis S. Modulation of hyaluronan signaling as a therapeutic target in human disease. Pharmacol Ther. 2022 Apr; 232: 107993. DOI: 10.1016/j.pharmthera.2021.107993. Epub 2021 Sep 26. PMID: 34587477; PMCID: PMC 8930430
- Gupta RC, Lall R, Srivastava A, Sinha A. Hyaluronic Acid: Molecular Mechanisms and Therapeutic Trajectory. Front Vet Sci. 2019 Jun 25; 6: 192. DOI: 10.3389/fvets.2019.00192. PMID: 31294035; PMCID: PMC 6603175
- Cowman MK, Schmidt TA, Raghavan P, Stecco A. Viscoelastic Properties of Hyaluronan in Physiological Conditions. F1000Res. 2015 Aug 25; 4: 622. DOI: 10.12688/f1000research.6885.1. PMID: 26594344; PMCID: PMC 4648226
- Dubrovin EV, Barinov NA, Ivanov DA, Klinov DV. Single‑molecule AFM study of hyaluronic acid softening in electrolyte solutions. Carbohydr Polym. 2023 Mar 1; 303: 120472. DOI: 10.1016/j. carbpol.2022.120472. Epub 2022 Dec 16. PMID: 36657830
- Liang J, Jiang D, Noble PW. Hyaluronan as a therapeutic target in human diseases. Adv Drug Deliv Rev. 2016 Feb 1; 97: 186–203. DOI: 10.1016/j.addr.2015.10.017. Epub 2015 Nov 2. PMID: 26541745; PMCID: PMC 4753080
- Campo GM, Avenoso A, Campo S, D'Ascola A, Nastasi G, Calatroni A. Small hyaluronan oligo- saccharides induce inflammation by engaging both toll‑like‑4 and CD 44 receptors in human chondrocytes. Biochem Pharmacol. 2010 Aug 15; 80 (4): 480–90. DOI: 10.1016/j.bcp.2010.04.024. Epub 2010 May 8. PMID: 20435021
- Ma SQ, Wei HL, Zhang X. TLR 2 regulates allergic airway inflammation through NF‑κB and MAPK signaling pathways in asthmatic mice. Eur Rev Med Pharmacol Sci. 2018 May; 22 (10): 3138–3146. DOI: 10.26355/eurrev_201805_15073. PMID: 29863259
- Scott JE, Cummings C, Brass A, Chen Y. Secondary and tertiary structures of hyaluronan in aque- ous solution, investigated by rotary shadowing‑electron microscopy and computer simulation. Hyaluronan is a very efficient network‑forming polymer. Biochem J. 1991 Mar 15; 274 (Pt 3) (Pt 3): 699–705. DOI: 10.1042/bj2740699. PMID: 2012600; PMCID: PMC 1149968
- Garantziotis S, Savani RC. Hyaluronan biology: A complex balancing act of structure, function, location and context. Matrix Biol. 2019 May;78–79:1–10. DOI: 10.1016/j.matbio.2019.02.002. Epub 2019 Feb 23. PMID: 30802498; PMCID: PMC 6774756
- Fraser JR, Laurent TC, Laurent UB. Hyaluronan: its nature, distribution, functions and turnover. J Intern Med. 1997 Jul; 242 (1): 27–33. DOI: 10.1046/j.1365–2796.1997.00170.x. PMID: 9260563
- Weng X, Maxwell‑Warburton S, Hasib A, Ma L, Kang L. The membrane receptor CD 44: novel insights into metabolism. Trends Endocrinol Metab. 2022 May; 33 (5): 318–332. DOI: 10.1016/j. tem.2022.02.002. Epub 2022 Mar 4. PMID: 35249813
- Misra S, Hascall VC, Markwald RR, Ghatak S. Interactions between Hyaluronan and Its Receptors (CD 44, RHAMM) Regulate the Activities of Inflammation and Cancer. Front Immunol. 2015 May 6; 6: 201. DOI: 10.3389/fimmu.2015.00201. PMID: 25999946; PMCID: PMC 4422082
- Tammi, R., Ågren, U. M., Tuhkanen, A.‑L., & Tammi, M. (1994). Hyaluronan Metabolism in Skin. Progress in Histochemistry and Cytochemistry, 29 (2), III‑77. DOI:10.1016/s0079–6336 (11) 80023‑9
- Jin C, Zong Y. The role of hyaluronan in renal cell carcinoma. Front Immunol. 2023 Mar 2;14:1127828. DOI: 10.3389/fimmu.2023.1127828. PMID: 36936902; PMCID: PMC 10019822.
- Papakonstantinou E, Roth M, Karakiulakis G. Hyaluronic acid: A key molecule in skin aging. Dermatoendocrinol. 2012 Jul 1; 4 (3): 253–8. DOI: 10.4161/derm.21923. PMID: 23467280; PMCID: PMC3583886
- Valachová K, Šoltés L. Hyaluronan as a Prominent Biomolecule with Numerous Applications in Medicine. Int J Mol Sci. 2021 Jun 30; 22 (13): 7077. DOI: 10.3390/ijms22137077. PMID: 34209222; PMCID: PMC 8269271
- Kawano Y, Patrulea V, Sublet E, Borchard G, Iyoda T, Kageyama R, Morita A, Seino S, Yoshida H, Jordan O, Hanawa T. Wound Healing Promotion by Hyaluronic Acid: Effect of Molecular Weight on Gene Expression and In Vivo Wound Closure. Pharmaceuticals (Basel). 2021 Mar 28; 14 (4): 301. DOI: 10.3390/ph14040301. PMID: 33800588; PMCID: PMC 8065935
- Jiang, Lei., Liu, Guihua., Liu, Hanyun., Han, Juan., Liu, Zhibin., & Ma, Hongchao., Molecular weight impact on the mechanical forces between hyaluronan and its receptor.Carbohydrate Polymers (2018), https://doi.org/10.1016/j.carbpol.2018.06.015
- Kobayashi Y, Okamoto A, Nishinari K. Viscoelasticity of hyaluronic acid with different molecular weights. Biorheology. 1994 May‑Jun; 31 (3): 235–44. DOI: 10.3233/bir‑1994–31302. PMID: 8729484
- Marcellin E, Steen JA, Nielsen LK. Insight into hyaluronic acid molecular weight control. Appl Microbiol Biotechnol. 2014 Aug; 98 (16): 6947–56. DOI: 10.1007/s00253–014–5853‑x. Epub 2014 Jun 24. PMID: 24957250
- Čožíková D, Šílová T, Moravcová V, Šmejkalová D, Pepeliaev S, Velebný V, Hermannová M. Preparation and extensive characterization of hyaluronan with narrow molecular weight distribution. Carbohydr Polym. 2017 Mar 15; 160: 134–142. DOI: 10.1016/j.carbpol.2016.12.045. Epub 2016 Dec 20. PMID: 28115087
- Хабаров В. Н. К вопросу о концентрации гиалуроновой кислоты в препаратах для биоре- витализации. Эстетическая медицина. 2015; 14 (1): 3–6.
Khabarov V. N. On the issue of hyaluronic acid concentration in biorevitalization preparations. Aesthetic medicine. 2015; 14 (1): 3–6. (In Russ.). - Brandt FS, Cazzaniga A. Hyaluronic acid gel fillers in the management of facial aging. Clin Interv Aging. 2008; 3 (1): 153–9. DOI: 10.2147/cia.s2135. PMID: 18488885; PMCID: PMC 2544360.
- Burdick JA, Prestwich GD. Hyaluronic acid hydrogels for biomedical applications. Adv Mater. 2011 Mar 25; 23 (12): H41–56. DOI: 10.1002/adma.201003963. Epub 2011 Mar 10. PMID: 21394792; PMCID: PMC 3730855
- Селянин М. А. [и др.]. Полисахариды в медицине будущего. Москва: Магистр‑Пресс, 2015. 254 с.
Selyanin M. A. [et al.]. Polysaccharides in medicine of the future. Moscow: Magistr‑Press, 2015. 254 p. (In Russ.). - Colon J, Mirkin S, Hardigan P, Elias MJ, Jacobs RJ. Adverse Events Reported From Hyaluronic Acid Dermal Filler Injections to the Facial Region: A Systematic Review and Meta‑Analysis. Cureus. 2023 Apr 29; 15 (4): e38286. DOI: 10.7759/cureus.38286. Erratum in: Cureus. 2023 Jun 30;15(6): c125. DOI: 10.7759/cureus.c125. PMID: 37261136; PMCID: PMC 10226824
- Trinh LN, Grond SE, Gupta A. Dermal Fillers for Tear Trough Rejuvenation: A Systematic Review. Facial Plast Surg. 2022 Jun; 38 (3): 228–239. DOI: 10.1055/s‑0041–1731348. Epub 2021 Jun 30. PMID: 34192769
- Jeong CH, Kim DH, Yune JH, Kwon HC, Shin DM, Sohn H, Lee KH, Choi B, Kim ES, Kang JH, Kim EK, Han SG. In vitro toxicity assessment of crosslinking agents used in hyaluronic acid dermal filler. Toxi- col In Vitro. 2021 Feb; 70: 105034. DOI: 10.1016/j.tiv.2020.105034. Epub 2020 Oct 20. PMID: 33096205
- Bondarenko I, Privalova E, Shumina Y. Sonography of the face and neck region soft tissues in assessment of the complications causes after facial contouring. Georgian Med News. 2021 Feb;(311):74–79. PMID: 33814395.
- Peros I, Haneke E. Fibrotic reaction to hyaluronic acid fillers in the face. J Cosmet Dermatol. 2024 Aug; 23 (8): 2543–2546. DOI: 10.1111/jocd.16419. Epub 2024 Jun 18. PMID: 38890804
- Селянин М. А. Избранные труды / М. А. Селянин. Москва: Магистр‑Пресс, 2015. 20 с. ISBN 978‑5‑89317‑237‑9.
Selyanin M. A. Selected works / M. A. Selyanin. Moscow: Magistr‑Press, 2015. 20 p. (In Russ.). ISBN 978‑5‑89317‑237‑9 - Mikhail A. Selyanin, Petr Ya, Vladimir N. Boykov, F. Polyak Khabarov, Hyaluronic acid: preparation, properties, in: Application in Biology And Medicine, 2015.
- Хабаров В. Н., Михайлова Н. П. Гиалуроновая кислота. Применение в косметологии и медицине. LAP LAMBERT Academic Publishing. 2012. 164 с.
Khabarov V. N., Mikhailova N. P. Hyaluronic acid. Application in cosmetology and medicine. LAP LAMBERT Academic Publishing. 2012. 164 p. (In Russ.). - Корякин С. Н., Иванов П. Л., Хабаров В. Н., Ядровская В. А., Исаева Е. В., Бекетов Е. Е., Зеле- нецкий А. Н., Успенский С. А., Селянин М. А., Ульяненко С. Е. Синтез и использование для нейтрон‑захватной терапии полихелатов гиалуроновой кислоты и бора‑10 // Химия. 2013; 47 (6): 14–18. DOI: https://doi.org/10.30906/0023‑1134‑2013‑47‑6‑14‑18
Koryakin S. N., Ivanov P. L., Khabarov V. N., Yadrovskaya V. A., Isaeva E. V., Beketov E. E., Zele- netsky A. N., Uspensky S. A., Selyanin M. A., Ulyanenko S. E. Synthesis and use of polychelates of hyaluronic acid and boron‑10 for neutron capture therapy // Chemistry. 2013; 47 (6): 14–18. (In Russ.). DOI: https://doi.org/10.30906/0023‑1134‑2013‑47‑6‑14‑18 - Saravanakumar K, Park S, Santosh SS, Ganeshalingam A, Thiripuranathar G, Sathiyaseelan A, Vijayasarathy S, Swaminathan A, Priya VV, Wang MH. Application of hyaluronic acid in tissue engineering, regenerative medicine, and nanomedicine: A review. Int J Biol Macromol. 2022 Dec 1; 222 (Pt B): 2744–2760. DOI: 10.1016/j.ijbiomac.2022.10.055. Epub 2022 Oct 12. PMID: 36243158
- Zhang Y, Sun T, Jiang C. Biomacromolecules as carriers in drug delivery and tissue engineering. Acta Pharm Sin B. 2018 Jan;8(1):34–50. DOI: 10.1016/j.apsb.2017.11.005. Epub 2017 Dec 9. PMID: 29872621; PMCID: PMC 5985630.
- Zainela Laborde López, Israel Alfonso Trujillo, Juan Carlos Rondón Rosell, Melvis Anaya Blanco, Pedro Ángel Tapia Diéguez, Olga García Benzal, Alicia María Tamayo Carbón, Eficacia y seguri- dad del ácido hialurónico en la eliminación de los signos de envejecimiento facial, Piel, Volume 36, Issue 10, 2021, Pages 641–647, ISSN 0213–9251, https://doi.org/10.1016/j.piel.2020.10.017